TMA-6
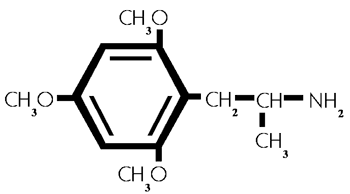
Formel aus:
(42)
Andere Namen:
2,4,6-Trimethoxyamphetamin. (42)
Allgemeines:
TMA-6 ist ein Halluzinogen. Es ist von der chemischen Struktur ein halluzinogenes Amphetamin und es ist nahe verwandt mit den anderen TMA�s. Es gibt eine Reihe von ihnen und das bekannteste ist die Verbindung TMA selbst. Die einzelnen TMA-Verbindungen unterscheiden sich nur durch die Lage ihre Methoxygruppen, wodurch sich auch die Wirkung der einzelnen TMA-Verbindungen etwas unterscheidet. Halluzinogene Amphetamine gibt es viele, wobei die bekanntesten vermutlich DOM (STP) und 2C-B sind. (42)
Alexander T. Shulgin fuehrt in seinem Werk noch folgende Kommentare an, die uebersetzt folgendermassen lauten:
TMA-6 ist einfach zu synthetisieren. Es ist eine der lohnendsten und angenehmsten von den Methoxyamphetaminen. Es ist gleich wirksam wie sein Gegenstueck TMA-2. Diese Verbindung, mit ihren 2,4,5-trisubstituierten Muster, hat als Schablone gedient, von der eine grosse Familie von sehr aktiven und faszinierenden Drogen weiterentwickelt wurde. Die 2,5-Dimethoxygruppen wurden intakt gelassen, und Veraenderungen in der 4.ten Position ergaben Schaetze wie DOM, DOB, DOET, DOI und die Alephverbindungen. Die ganze Welt der 2C-X's-Halluzinogene hat diese Orientierung der 2,5-Dimethoxygruppen. (42)
Die Position 4 ist bei den 2C-X-Halluzinogenen jeweils mit verschiedenen Molekuelgruppen besetzt. Beispielsweise ist bei 2C-B das Atom Brom an dieser Stelle und bei 2C-C Chlor. (eigen)
A. Shulgin fuehrt weiters in seinem Buch "PHIKAL" aus:
Hier gibt es den eklatanten, parallelen Ruf von TMA-6. Es kann als 2,4,6-Gegenstueck dienen, als eine aehnliche Schablonenverbindung. Die ersten Anzeichen sind, dass wenn man die 2,6-Dimethoxygruppen intakt laesst, eine komplett analoge Serie gemacht werden koennte, wieder mit Aenderungen in der 4.ten Position. Diese wurden benannt als die psu-Serie, oder psi-Serie, als Abkuerzung fuer das Prefix, pseudo, und koennen unterschieden werden von den 2,4,5-Dingen mit dem Gebrauch des griechischen Buchstaben 'Y', So gibt es das Y-DOM (auch Z-7 genannt, sicherlich eine aktive Verbindung), und Y-DOB, Y-DOET, Y-DOI, und die Y-ALEPH Verbindungen. Und natuerlich die Y-2C-X Gegenstuecke. Ich wuerde erwarten, dass alle aktiv und sicherlich einige interessant sind. Sie werden betraechtlich schwerer zu synthetisieren sein. Wie dem auch sei, einige von ihnen, speziell Dinge wie Y-2C-T-4, sind schon bereitet und getestet worden. (42)
Dosis:
Die Dosis zur Erreichung eines veraenderten Bewu�tseinszustandes betraegt nach A. Shulgin 25-50 mg. (42)
Wirkdauer:
A. Shulgin gibt die Dauer der Wirkung mit 12-16h an. (42)
Wirkungen:
A. Shulgin gibt folgende subjektiven Erfahrungsberichte ueber die halluzinogene Rauschdroge TMA-6 in seinem Buch "PHIKAL" an:
35 mg: Mein Koerper war ganz und gar kribbelig. Es gab Zeiten, in denen das Gehen unsicher war. Denken war ein wenig schwierig, ebenso war ich ausgesprochen vergiftet das meiste vom Tag (den ganzen Tag, wenn ich mir es nun ueberlege). Etwas zu tun, wie das Toasten des Toasts im Toaster, war schwierig. Und die Dinge waren so lustig die meiste Zeit. Den Tisch fuers Abendessen zu decken, 6h spaeter, war sehr vergnueglich. Wir waren alle beim Schlafengehen vergiftet, was fuer eine Zeit es auch war. Ich hatte eine schwierige Zeit beim Schlafen. Wenn ich es wiederholen wuerde, wuerde ich eine niedrigere Dosis waehlen, fuehle ich. (42)
40 mg: Dieses Experiment begann zu mittag eines kalten, verregneten Tages. Beinahe der ganze Tag musste innerhalb des Hauses verbracht werden, ohne den Vorteil von Sonnenschein. Dies ist es wert erwaehnt zu werden, weil es ein entschiedenes Gefuehl innerer Kaelte in den ersten 8h des Experiments gab, dass nicht so stark erschienen waere, wenn es ein warmer Tag gewesen waere. Die meisten, wenn nicht alle, von den anderen 8 Teilnehmern berichteten ebenso von der gleichen Kaelte. Es gab etwas visuelles Funkeln, dass durchwegs anhielt. In der zweiten Stunde kam ein geringe aber anhaltende Magenuebelkeit auf, eingeleitet von einer Durchfall-aehnlichen Darmbewegung. Es gab keine Beeintraechtigung des Sprechens, aber es gab etwas Anhaltendes bei allen Denkprozessen. Es war einfach ueber persoenliche Dinge zu reden, aber es scheint keine bedeutende Einsichtssteigerung zu geben. Der Appetit war erniedrigt. Schlaf war entschieden schwierig, nachdem die Wirkungen der Droge im uebrigen aufgehoert hatten. (42)
50 mg: Mein frueherer Versuch mit dieser Dosis erzeugte eine Note, die besagte: 'Veraenderung des Bewusstseins, aber nichts Visuelles, nicht irgendwas', und - Ueberraschung! Es war sehr, sehr aktiv, visuell, farbenfroh, ... Gutes Reden, klare und sichere Koerperkontrolle, trotz intensiven Engergiefluss'. Sehr lustig - grossartiger Humor, wundervolles Lachen. (42)
Sucht:
Die Ausbildung einer koerperlichen Abhaengigkeit ist nicht bekannt. (eigen)
Synthese:
A. Shulgin gibt folgendes Herstellungsverfahren in seinem Werk "PHIKAL" an:
Zu einer Loesung von 100g Phloroglucinoldihydrat in 320 ml MeOH wurden 55ml konz. H2SO4 zugefuegt. Die klare Loesung wurde uebernacht am Rueckfluss gehalten. Nach dem Abkuehlen wurden 500 ml H2O zugefuegt. Der Hauptteil vom MeOH wurde im Vakuum entfernt. Das restliche Oel wurde mit Et2O extrahiert. Entfernen von diesem, liess 60g rotes Oel als Rest zurueck. Dieser wurde in 300g Methylsulfat geloest (Vorsicht, dieses ist extrem giftig bei Hautkontakt. Jede Kontaktstelle muss durch und durch mit verd. Ammoniumhydroxid gewaschen werden). Unter gutem Ruehren, wurde dies vorsichtig mit 500g 40%-igem, waessrigen KOH versetzt. Die exotherme Reaktion liess man laufen. Extraktion mit 3x100 ml Et2O gab, nach Verdunsten des Loesungsmittel von den vereinten Extrakten, ein Oel, dass grossteils kristallin wurde. Dieses wurde in 100 ml Hexan suspendiert, und durch eine grobe Glasfilternutsche filtriert. Durch Verdunsten wurden 57g 1,3,5-Trimethoxybenzol erhalten, als blass bernsteinfarbener Feststoff, der bei 44-50 Grad Celsius schmolz. Ein Beispiel, gereinigt durch Umkristallisieren aus EtOH, hatte den passenden mp von 54-55 Grad Celsius.
Einer Mischung von 62.9g N-Methylformanilid und 71.3g POCl3 wurde es erlaubt eine halbe Stunde zu stehen, was eine leicht weinrote Farbe produzierte. Es wurden dann 30.9g 1,3,5-Trimethoxybenzol hinzugefuegt. Die Mischung wurde am Dampfbad 2h lang erhitzt. Die Reaktionsmischung wurde dann in zerkleinertes Eis gegossen, und einige Stunden lang geruehrt. Die dunkle, gummige Masse wurde mit 2x100 ml Et2O extrahiert (dies wurde verworfen) und dann mit 4x200 ml CH2Cl2. Die letzteren Extrakte wurden vereint. Das Loesungsmittel wurde im Vakuum entfernt. Es gab eine Ausbeute von 14g bernsteinfarbenen Feststoff. Dieser wurde aus 80 ml kochendem MeOH (es wurde entfaerbende Aktivkohle gebraucht und die kochende Loesung wurde durch Papier filtriert) umkristallisiert, um 10g 2,4,6-Trimethoxybenzaldehyd, als einen weissen, kristallinen Feststoff mit einem mp von 115-116 Grad Celsius, zu ergeben. Die Literaturwerte sind allgemein 1 Grad Bereiche. Sie sind gleich 121 Grad Celsius. Das Malonnitriladditionsprodukt wurde aus einer Loesung von 0.5g Aldehyd und 0.5g Malononitril in 10 ml warmen MeOH bereitet, und mit einem Tropfen Triethylamin behandelt. Es gab sofort eine Bildung einer gelben, kristallinen Masse, welche durch Filtration entfernt, mit EtOH gewaschen, und an der Luft getrocknet wurde. Die Ausbeute an 2,4,6-Trimethoxybenzalmalononitril war 0.5g. Der mp war bei 174-175 Grad Celsius.
Eine Loesung von 5g 2,4,6-Trimethoxybenzaldehyd in 20g Nitroethan wurde mit 1g wasserfreiem Ammoniumacetat versetzt und 24h am Dampfbad belassen. Ueberschuessige Loesungsmittel/Reagenzien wurden von der tiefrot gefaerbten Loesung im Vakuum entfernt. Es gab einen Rest, der ploetzlich zu einer kristallinen Masse wurde. Diese wurde gut unter 5ml MeOH gemahlen, filtriert, und mit 3ml zusaetzlichem MeOH gewaschen, was 5.4g 2-Nitro -1- (2,4,6-trimethoxyphenyl) propen, als gelbe Kristalle, ergab. Der mp von diesem rohen Material war 135-142 Grad Celsius, welcher auf 147-148 Grad Celsius, durch Umkristallisieren aus EtOH, gehoben werden konnte. Der Gebrauch einer alternativen Synthese dieses Nitrostyrens, die Essigsaeure als Loesungsmittel und eine stoechiometrische Menge Nitroethan (und Ammoniumacetat als Katalysator) benutzte, ergab sehr geringe Ausbeuten. Der Einsatz von Butylamin als Katalysator ergab betraechtlich bessere Ergebnisse.
Eine Suspension von 50g LAH in 1l wasserfreiem THF wurde in eine Inertatmosphaere gegeben, magnetisch geruehrt, und zu einem sanftem Kochen am Rueckfluss gebracht. Es wurde 56.9g 2-Nitro -1- (2,4,6-trimethoxyphenyl) propen, als eine gesaettigte Loesung in THF, hinzugefuegt. Dies wurde erreicht, indem man das kondensierte THF durch einen Soxhletaufsatz troepfeln liess, der das Nitrostyren beinhaltete, mit direkter Addition zur Reaktionsmischung. Die Loeslichkeit war extrem niedrig. Die geruehrte Mischung wurde 36h am Rueckfluss gehalten. Eine weiche, cremige, graue Farbe bildete sich. Nachdem auf Zimmertemperatur abgekuehlt war, wurde das ueberschuessige Hydrid durch vorsichtige Addition von 50 ml H2O, gefolgt von 50 ml 15%-iger NaOH (es entwickelte sich immer noch einige Hitze), und 150 ml zusaetzlichem H2O, zerstoert. Das Ruehren wurde forgesetzt, bis die unloeslichen Salze weiss und locker waren. Diese Feststoffe wurden durch Filtration entfernt. Der Filterkuchen wurde mit zusaetzlichem THF gewaschen. Die vereinten Filtrate und Waschungen wurden vom Loesungsmittel im Vakuum befreit. Die 73g blass bernsteinfarbener Rest wurden in 200 ml IPA geloest, mit annaehernd 50 ml konz. HCl neutralisiert, und mit 2l wasserfreiem Et2O verduennt. Eine untere, oelige Phase trennte sich, die langsam eine kristalline Masse bildete. Diese wurde durch Filtration entfernt, mit Et2O gewaschen, und an der Luft bis zu einem konstanten Gewicht getrocknet. Das Gewicht an 2,4,6-Trimethoxyamphetaminhydrochlorid war 41.3g. Die Farbe war gebrochen weiss. Es gab eine Tendenz zum Verfaerben bei Luftkontakt. Der mp war bei 204-205 Grad Celsius, der auf 207-208 Grad Celsius, nach Umkristallisieren aus IPA, gesteigert wurde. Die Literatur gibt einen mp von 214-215 Grad Celsius fuer dieses Salz, nach Isolation und Reinigung als Pikratsalz (mit einem mp 212-213 Grad Celsius aus EtOH), an. (42)